研究背景:脑卒中治疗的“最后一公里”困境
脑卒中是全球范围内导致死亡和残疾的主要原因之一。尽管开发了多种神经保护剂,但其临床转化效果普遍不佳。核心瓶颈在于血脑屏障(BBB)——一个高度选择性的生理屏障,它在保护大脑的同时,也阻碍了超过98%的药物进入脑实质。因此,如何开发能够精准“导航”并高效“穿越”血脑屏障的智能药物递送系统,成为该领域亟待突破的关键科学问题。
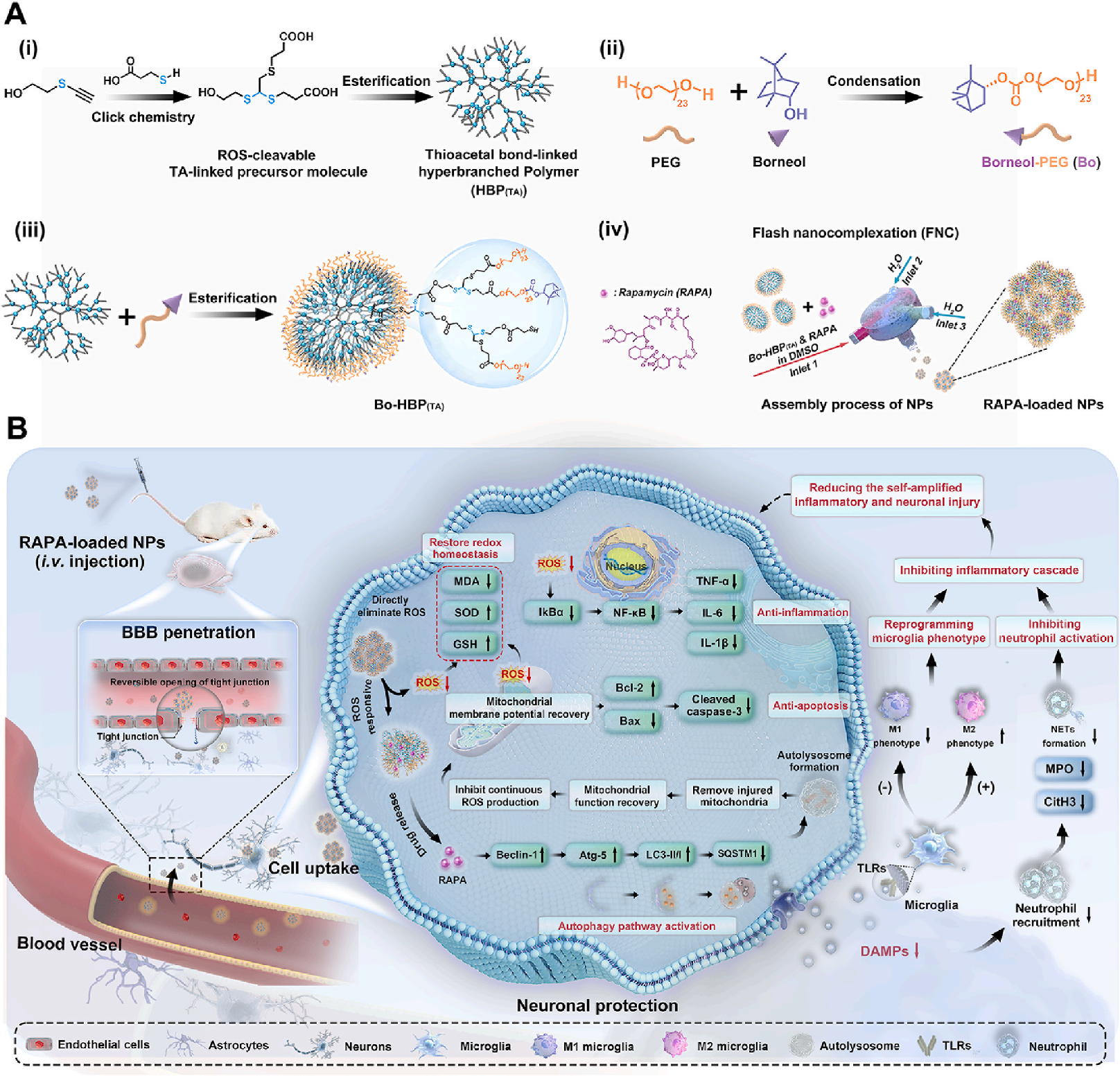
技术路径解析与科辰星飞解决方案
为应对挑战,研究团队构建了一种基于ROS响应性超支化聚合物的纳米粒。这种纳米粒表面修饰了脑靶向分子“冰片”(Borneol),使其能够主动穿越血脑屏障。进入缺血区域后,病灶处高水平的活性氧(ROS)会触发纳米粒结构解体,从而精准、按需地释放内部包裹的治疗药物雷帕霉素。这一精巧设计的有效性,必须通过可靠的体内示踪技术来验证。研究人员需要清晰地看到纳米粒是否真的如预期那样大量富集于脑部,而非其他器官。
在本研究中,研究人员明确采用了“a multifunctional fluorescence imaging system (LumiFluor AVIS T II, KoreshineFaye, China)”来完成这一关键验证。这充分证明了科辰星飞的LumiFluor AVIS T 小动物活体成像系统,凭借其高灵敏度的CCD相机和先进的光学设计,能够捕捉到深层组织(如脑部)发出的微弱荧光信号,为小鼠活体荧光成像提供了卓越的图像质量和精准的定量分析能力,是验证新型靶向药物递送效率的理想工具。
使用 LumiFluor AVIS T 小动物活体成像系统 复现实验核心步骤
- 第一步:模型与探针准备。构建大脑中动脉栓塞(MCAO)的缺血性脑卒中小鼠模型。将具有近红外荧光的DiR染料装载于靶向纳米粒(Bo-HBP(TA)@DiR)中,通过尾静脉注射给药。
- 第二步:离体器官成像。在注射后不同时间点(1, 3, 6, 9, 12小时),处死小鼠,快速、完整地取出大脑、心脏、肝、脾、肺、肾等主要器官,整齐排列于成像舱内。
- 第三步:图像采集与定量分析。启动LumiFluor AVIS T活体成像系统,选择合适的近红外滤光片和曝光参数进行荧光成像。采集完成后,使用配套的分析软件圈定感兴趣区域(ROI),对各器官的荧光信号强度进行定量,最终计算出纳米粒在各器官的生物分布(%ID/g)。
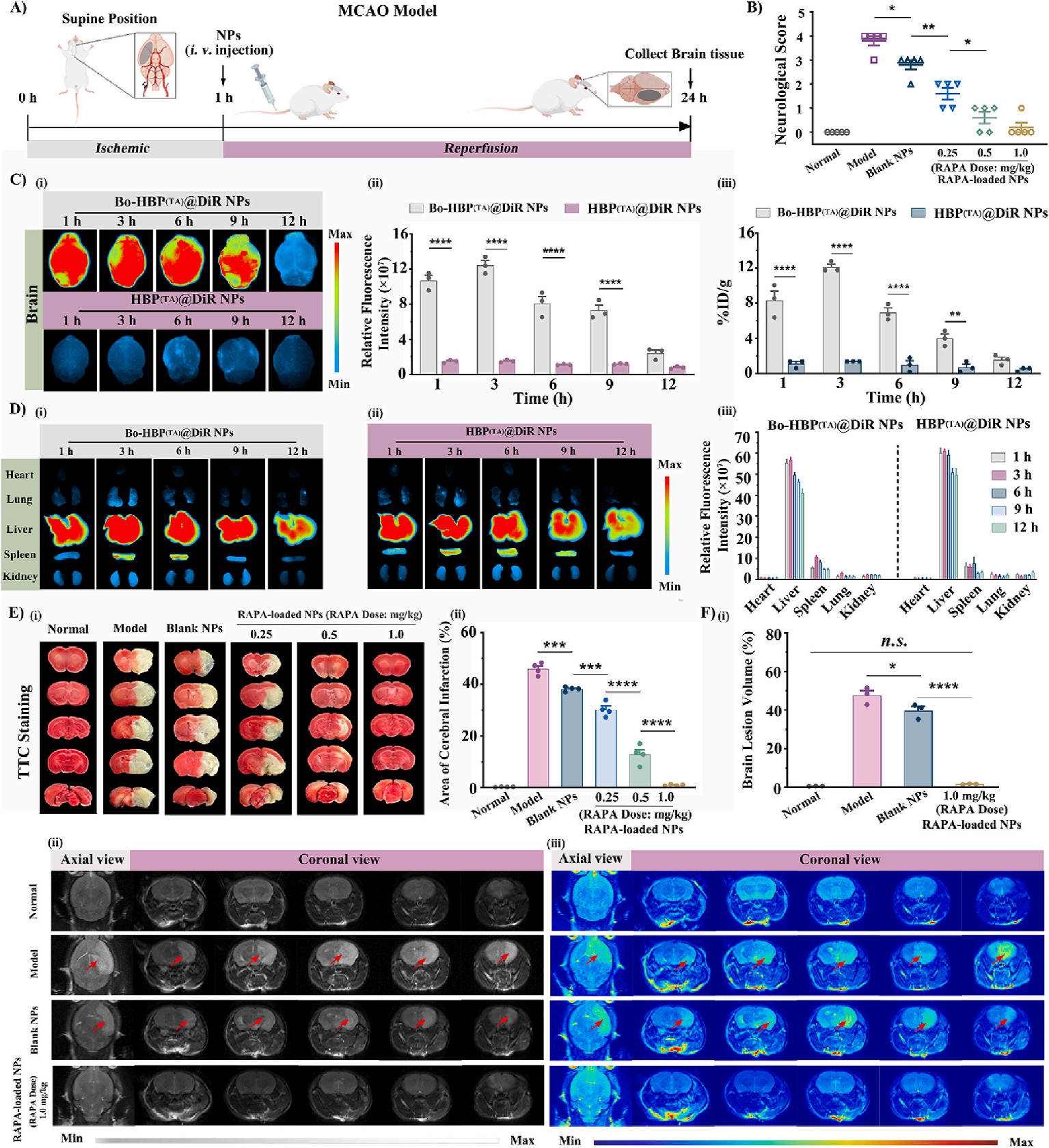
关键成果与意义
该研究构建的动态响应纳米系统,不仅实现了前所未有的脑部靶向效率,还将梗死面积从46.2%降至惊人的1.1%,为缺血性脑卒中的治疗提供了极具临床转化潜力的全新策略。
这项发表于《Biomaterials》的重磅研究,不仅为脑卒中治疗提供了创新的解决方案,也再次凸显了先进的国产小动物活体成像技术在生命科学前沿探索中的关键作用。科辰星飞的活体成像系统,能够为研究人员提供可靠、直观、可定量的体内数据,是推动药物研发、疾病机理研究等领域不断取得突破的强大助力。