研究背景:中大与港科大联手攻克AKI治疗难题
急性肾损伤(AKI)是临床常见的危重病症。近日,由中山大学(Sun Yat-sen University)生物医学工程学院的曹中教授、赵毅教授团队,联合香港科技大学(HKUST)的吴军教授团队,共同开发了一种新型单宁酸-铈纳米酶(TA-Ce)。这种纳米药物旨在通过模拟SOD和CAT等抗氧化酶的活性,清除体内过量的活性氧(ROS),从而缓解肾脏损伤。

技术挑战:如何看见药物在“受损肾脏”中的行踪?
在这一高水平研究中,单纯的生化指标不足以解释药物的起效机制。研究团队需要回答:纳米颗粒是否真的到达了肾脏?其在受损组织(AKI模型)中的积累是否由于血管通透性增加而有所不同?传统的解剖切片只能提供静态快照,无法满足顶刊对于数据直观性和动态性的高要求。因此,小动物活体成像技术成为了该课题组不可或缺的分析手段。
解决方案:科辰星飞 LumiFluor 系统助力名校科研
该联合研究团队使用了 科辰星飞(Koreshine Faye)提供的 LumiFluor AVIS 小动物活体成像系统 来执行关键的生物分布(Biodistribution)实验。
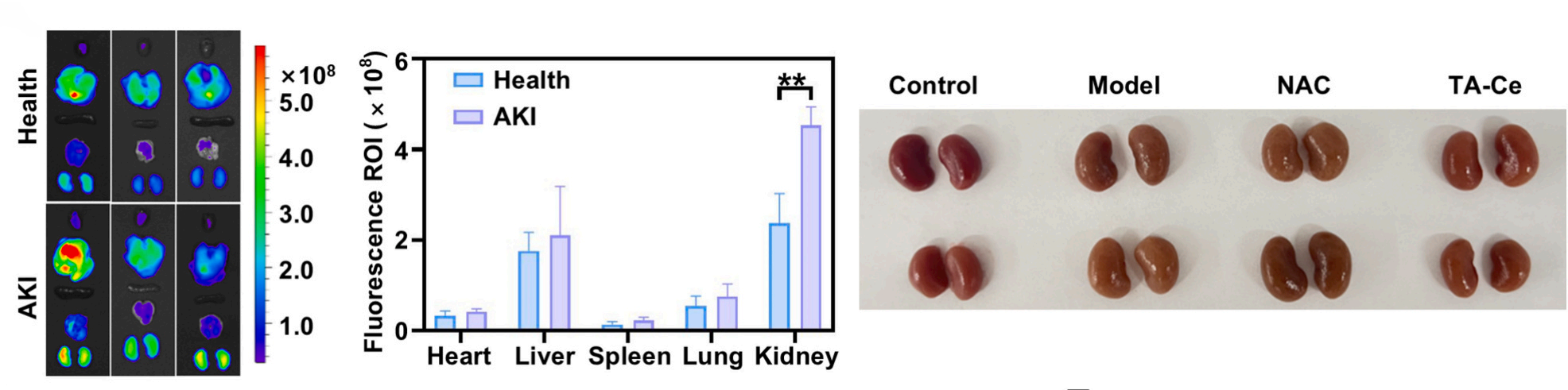
研究人员给患有横纹肌溶解诱导AKI的小鼠静脉注射了荧光标记的TA-Ce。在 LumiFluor 系统的高灵敏度镜头下,药物在体内的分布一览无余。成像结果清晰地显示,在注射后6小时,AKI小鼠肾脏部位的荧光信号显著强于健康对照组。这一发现强有力地支持了纳米酶能够利用病理环境下的增强渗透与滞留(EPR)效应靶向治疗肾损伤的假设。
使用 LumiFluor AVIS T 复现中大团队实验步骤
- 荧光探针制备:参考文中方法,合成RhB标记的TA-Ce纳米复合物,确保荧光基团稳定结合。
- 模型构建与给药:构建RM-AKI小鼠模型,并于禁水禁食后通过尾静脉注射标记药物(15 mg/kg)。
- 活体/离体成像:使用 LumiFluor AVIS T 系统,在注射后6小时对小鼠进行活体成像;随后取心、肝、脾、肺、肾进行离体成像(Ex vivo imaging),以获得无背景干扰的脏器荧光分布图。
- 数据定量:利用系统软件圈选肾脏区域(ROI),量化平均辐射效率,并计算“AKI组”与“健康组”的信号比值,验证靶向性。
顶刊成果与行业启示
“该研究证实,TA-Ce 不仅具有良好的生物相容性,还能在受损肾脏中有效积累,其积累量约为健康组织的2倍,这得益于LumiFluor系统提供的精确影像学证据。”
中山大学与香港科技大学的这项研究不仅为AKI治疗提供了新策略,也再次证明了科辰星飞小动物活体成像系统在高端生物医学研究中的可靠性。无论是药代动力学追踪还是靶向性验证,我们的设备都能协助顶尖科研团队产出高质量的数据。